Calor Latente – Trocas de calor com mudança de estado
Exercícios de vestibulares com resolução comentada sobre
Calor Latente – Trocas de calor com mudança de estado
01-(UFB) Determine a quantidade de calor que se deve fornecer a 100g de gelo a -10oC para transformá-lo em vapor a 110oC. Esboce a curva de aquecimentodo processo.
Dados: calor específico da água = 1,0 cal/g °C — calor específico do gelo = calor específico do vapor=0,5 cal/g °C — calor latente de fusão do gelo = 80 cal/g — calor latente de vaporização da água=540cal/g
02-(PUC-SP)
O gráfico da quantidade de calor absorvida por um corpo de massa 5g, inicialmente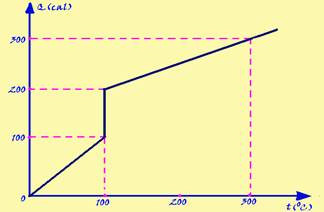
líquido, em função da temperatura T, em uma transformação sofrida por esse corpo, é dado pela figura.
a) Qual o calor latente de mudança de fase?
b) Qual o calor específico da substância no estado líquido?
03-(FUVEST-SP) O gráfico representa, em função do tempo, a leitura de um termômetro que mede a
temperatura de uma substância inicialmente no estado sólido, contida num recipiente. O conjunto é aquecido uniformemente numa chama de gás, a partir do instante zero; depois de algum tempo o aquecimento é desligado. A temperatura de fusão da substância é, em oC: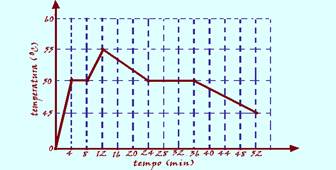
a) 40
b) 45
c) 50
d) 53
e) 55
04-(UFU-MG) Na aula de Física, o professor Chico Boca entrega aos estudantes um gráfico da variação da temperatura (em °C) em função do calor fornecido (em calorias). Esse gráfico, apresentado a seguir, é referente a um experimento em que foram aquecidos 100 g de gelo, inicialmente a -20°C, sob pressão atmosférica constante.
Em seguida, o professor solicita que os alunos respondam algumas questões. Auxilie o professor na elaboração do gabarito correto calculando, a partir das informações dadas,
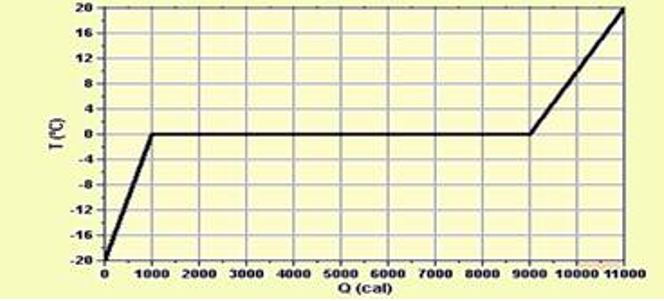
a) o calor específico do gelo;
b) o calor latente de fusão do gelo;
c) a capacidade térmica da quantidade de água resultante da fusão do gelo.
05-(ENEM-MEC) A Terra é cercada pelo vácuo espacial e, assim, ela só perde energia ao irradiá-la para o espaço.
O aquecimento global que se verifica hoje decorre de pequeno desequilíbrio energético, de cerca de 0,3%, entre a energia que a Terra recebe do Sol e a energia irradiada a cada segundo, algo em torno de 1 W/m2. Isso significa que a Terra acumula, anualmente, cerca de 1,6 × 1022 J. Considere que a energia necessária para transformar 1 kg de gelo a 0°C em água líquida seja igual a 3,2 × 105 J. Se toda a energia acumulada anualmente fosse usada para derreter o gelo nos pólos (a 0°C), a quantidade de gelo derretida anualmente, em trilhões de toneladas, estaria entre
a) 20 e 40.
b) 40 e 60.
c) 60 e 80.
d) 80 e 100.
e) 100 e 120.
06-(PUC-PR) Uma fonte de energia (térmica), de potência constante e igual a 20 cal/s, fornece calor a uma massa sólida de 100 g.

O gráfico a seguir mostra a variação de temperatura em função do tempo:
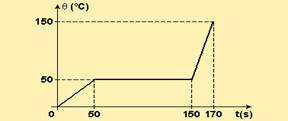
Marque a alternativa correta:
a) O calor latente de fusão da substância é de 200 cal/g.
b) A temperatura de fusão é de 150° C.
c) O calor específico no estado sólido é de 0,1 cal/g° C.
d) O calor latente de fusão é de 20 cal/g.
e) O calor específico no estado líquido é de 0,4 cal/g° C.
07-(UnB-DF) Uma dona de casa residente em Brasilia, precisando ferver água, resolveu utilizar um ebulidor (vulgarmente conhecido como “mergulhão) ou “rabo quente”, que é um equipamento elétrico capaz de fornecer energia calorífica ao líquido noqual se encontra imerso. Colocou, então, o ebulidor em um recipiente contendo 2,5 litros de água a 18oC, ligando-o em seguida. Por um descuido, após atingir a temperatura de ebulição de 96oC, parte da água vaporizou. Ao desligar o ebulidor, a dona de casa constatou que, naquele instante, restava apenas 1,5 litros de água. Sabendo que o calor específico da água é 1,0 cal/goC, e que a densidade da água é 1g/cm3, bem como o clor latente de vaporização da água igual a 540 cal/g, e que 1 cal equivale a 4,2J e também que a potência do ebulidor era de 1.000W. e considerando desprezível as trocas de calor com o ambiente e o tempo de aquecimento do ebulidor, calcule, em minutos, o tempo em que o ebulidor permaneceu ligado. Despreze a parte fracionária de seu resultado, caso exista. 
08-(FUVEST-SP) Um recipiente de isopor, que é um bom isolante térmico, tem em seu interior água e gelo em equilíbrio térmico. Num dia quente, a passagem de calor por suas paredes pode ser estimada, medindo-se a massa de gelo Q presente no interior do isopor, ao longo de algumas horas, como representado no gráfico.
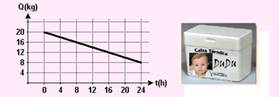
Esses dados permitem estimar a transferência de calor pelo isopor, como sendo, aproximadamente, de
Calor latente de fusão do gelo ¸ 320 kJ/kg
a) 0,5 kJ/h
b) 5 kJ/h
c) 120 kJ/h
d) 160 kJ/h
e) 320 kJ/h
09-(FUVEST-SP) As curvas A e B na figura representam a variação da temperatura (θ) em função do tempo(t) de duas substâncias A e B, quando 50g de cada uma é aquecida separadamente, a partir da temperatura de 20oC, na fase sólida, recebendo calor numa taxa constante de 20 cal/s.
Considere agora um experimento em que 50 g de cada uma das substâncias são colocados em contato térmico num recipiente termicamente isolado, com a substância A na temperatura inicial θA=280oC e a substância B na temperatura inicial θB=20oC.
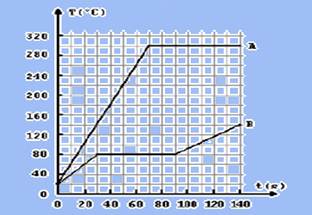
a) Determine o valor do calor latente de fusão LB da substância B.
b) Se a temperatura final corresponder à mudança de fase de uma das substâncias, determine a quantidade dela em cada uma das fases.
10-(UNESP-SP) A figura mostra os gráficos das temperaturas em função do tempo de aquecimento, em dois experimentos separados, de dois sólidos, A e B, de massas iguais, que se liquefazem durante o processo. A taxa com que o calor é transferido no aquecimento é constante e igual nos dois casos.
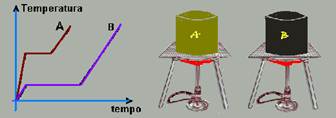
Se TA e TB forem as temperaturas de fusão e LA e LB os calores latentes de fusão de A e B, respectivamente, então
a) TA > TB e LA > LB.
b) TA > TB e LA = LB.
c) TA > TB e LA < LB.
d) TA < TB e LA > LB.
e) TA < TB e LA = LB.
11-(Olimpíada Brasileira de Física) Dentro de um recipiente existem 2.400g de água e um pedaço de gelo. O recipiente é colocado no fogão em uma chama branda que fornece calor a uma razão constante. A temperatura foi monitorada durante 80 minutos e o resultado é o representado no gráfico.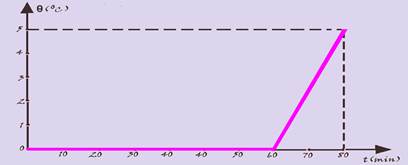
O calor latente de fusão do gelo é 80 cal/g e o calor específico da água líquida é 1 cal/goC. Calcule:
a) a massa inicial do gelo
b) a taxa de calor transferida ao sistema por minuto.
12-(PUC-RJ) Um calorímetro isolado termicamente possui, inicialmente, 1,0 kg de água a uma temperatura de 55 °C.

Adicionamos, então, 500 g de água a 25 °C. Dado que o calor especifico da água é 1,0 cal/(g.°C), que o calor latente de fusão é 80 cal/g e que sua densidade é 1,0 g/cm3, calcule:
a) a temperatura de equilíbrio da água;
b) a energia (em calorias – cal) que deve ser fornecida à água na situação do item a) para que esta atinja a temperatura de ebulição de 100 °C
c) quanto calor deve ser retirado do calorímetro, (no item b), para que toda a água fique congelada.
13-(FUVEST-SP) Quando água pura é cuidadosamente resfriada, nas condições normais de pressão, pode permanecer no estado líquido até temperaturas inferiores a 0°C, num estado instável de “superfusão”. Se o sistema é perturbado, por exemplo, por vibração, parte da água se transforma em gelo e o sistema se aquece até se estabilizar em 0°C. O calor latente de fusão da água é L = 80 cal/g.
Considerando-se um recipiente termicamente isolado e de capacidade térmica desprezível, contendo um litro de água a –5,6°C, à pressão normal, determine:
a) A quantidade, em g, de gelo formado, quando o sistema é perturbado e atinge uma situação de equilíbrio a 0°C.
b) A temperatura final de equilíbrio do sistema e a quantidade de gelo existente (considerando-se o sistema inicial no estado de “superfusão” a –5,6ºC), ao colocar-se, no recipiente, um bloco metálico de capacidade térmica C=400cal/ºC, na temperatura de 91°C.
14-(FUVEST-SP) Um aquecedor elétrico é mergulhado em um recipiente com água a 10 °C e, cinco minutos depois, a água começa a ferver a 100 °C. Se o aquecedor não for desligado, toda a água irá evaporar e o aquecedor será danificado. Considerando o momento em que a água começa a ferver, a evaporação de toda a água ocorrerá em um intervalo de aproximadamente
Calor específico da água = 1,0 cal/(g°C)
Calor de vaporização da água = 540 cal/g
Desconsidere perdas de calor para o recipiente, para o ambiente e para o próprio aquecedor.
a) 5 minutos.
b) 10 minutos.
c) 12 minutos.
d) 15 minutos.
e) 30 minutos.
15-(UFG-GO) Num piquenique, com a finalidade de se obter água gelada, misturou-se num garrafão térmico, de capacidade térmica desprezível, 2kg de gelo picado a 0°C e 3kg de água que estavam em garrafas ao ar livre, à temperatura ambiente de 40oC

Desprezando-se a troca de calor com o meio externo e conhecidos o calor latente de fusão do gelo (80 cal/g) e o calor específico da água (1 cal/g°C), a massa de água gelada disponível para se beber, em kg, depois de estabelecido o equilíbrio térmico, é igual a
![]()
16-(ITA-SP) Durante a realização de um teste, colocou-se 1 litro de água a 20 °C no interior de um forno de micro-ondas.
Após permanecer ligado por 20 minutos, restou meio litro de água. Considere a tensão da rede de 127 V e de 12 A a corrente consumida pelo forno. Calcule o fator de rendimento do forno.
Dados: calor de vaporização da água LV = 540 cal/g; calor específico da água c = 1 cal/g°C; 1 caloria = 4,2 joules.
17-(UNIFESP-SP) A enfermeira de um posto de saúde resolveu ferver 1,0 litro de água para ter uma pequena reserva de água esterilizada. Atarefada, ela esqueceu a água a ferver e quando a guardou verificou que restaram 950 mL.
Sabe-se que a densidade da água é 1,0 .103 kg/m3, o calor latente de vaporização da água é 2,3 . 106 J/kg e supõe-se desprezível amassa de água que evaporou ou possa ter saltado para fora do recipiente durante a fervura. Pode-se afirmar que a energia desperdiçada na transformação da água em vapor foi aproximadamente de:
a) 25 000 J.
b) 115 000 J.
c) 230 000 J.
d) 330 000 J.
e) 460 000 J.
18-(UFMG-MG) Em uma aula no Laboratório de Física, o Professor Jésus realiza o experimento que se descreve a seguir.
Inicialmente, ele imerge um aquecedor elétrico em 1,0 kg de água, à temperatura de 23 °C, contida num recipiente de isopor. Em seguida, o recipiente é tampado e o aquecedor é ligado, até a temperatura da água atingir 45 °C.
Considere que a tensão e a corrente elétricas, no aquecedor, são, respectivamente, de 220 V e de 1,0 A. Despreze a capacidade térmica do recipiente e a do aquecedor.
a) Com base nessas informações, CALCULE o tempo que o aquecedor ficou ligado. Sabe-se que o calor específico da água é 4,2.103 J/kg.oC
b) Em seguida, o Professor Jésus coloca 0,60 kg de gelo, a 0,0 °C, na água contida no recipiente, tampa-o novamente, e espera até a temperatura dela se estabilizar. Sabe-se que o calor latente de fusão do gelo é de 3,3 × 105 J/kg. Considerando essas informações, CALCULE a temperatura da água no final desse experimento.
19-(FUVEST-SP) Um roqueiro iniciante (Marcus Lipas) improvisa efeitos especiais, utilizando gelo seco (CO2sólido) adquirido em uma fábrica de sorvetes. Embora o início do show seja à meia-noite (24 h), ele o compra às 18 h, mantendo-o em uma “geladeira” de isopor, que absorve calor a uma taxa de, aproximadamente, 60 W, provocando a sublimação de parte do gelo seco.
Para produzir os efeitos desejados, 2 kg de gelo seco devem ser jogados em um tonel com água, a temperatura ambiente, provocando a sublimação do CO2 e a produção de uma “névoa”. A parte visível da “névoa”, na verdade, é constituída por gotículas de água, em suspensão, que são carregadas pelo CO2 gasoso para a atmosfera, à medida que ele passa pela água do tonel. Estime:
a) A massa de gelo seco, Mgelo, em kg, que o roqueiro tem de comprar, para que, no início do show, ainda restem os 2 kg necessários em sua “geladeira”.
b) A massa de água, Mágua, em kg, que se transforma em “névoa” com a sublimação de todo o CO2, supondo que o gás, ao deixar a água, esteja em CNTP, incorporando 0,01 g de água por cm3 de gás formado.
NOTE E ADOTE:
Sublimação: passagem do estado sólido para o gasoso.
Temperatura de sublimação do gelo seco = – 80 °C.
Calor latente de sublimação do gelo seco = 648 J/g.
Para um gás ideal, PV = nRT.
Volume de 1 mol de um gás em CNTP = 22,4 litros.
Massa de 1 mol de CO2 = 44 g.
Suponha que o gelo seco seja adquirido a – 80 °C.
20-(ENEM-MEC) A água apresenta propriedades físico-químicas que a coloca em posição de destaque como substância essencial à vida. Dentre essas, destacam-se as propriedades térmicas biologicamente muito importantes, por exemplo, o elevado valor de calor latente de vaporização. Esse calor latente refere-se à quantidade de calor que deve ser adicionada a um líquido em seu ponto de ebulição, por unidade de massa, para convertê-lo em vapor na mesma temperatura, que no caso da água é igual a 540 calorias por grama.
A propriedade físico-química mencionada no texto confere à água a capacidade de
a) servir como doador de elétrons no processo de fotossíntese.
b) funcionar como regulador térmico para os organismos vivos.
c) agir como solvente universal nos tecidos animais e vegetais.
d) transportar os íons de ferro e magnésio nos tecidos vegetais.
e) funcionar como mantenedora do metabolismo nos organismos vivos.
21-(UNESP-SP) Ao ser anunciada a descoberta de novo planeta em torno da estrela Gliese581 e a possível presença de água na fase líquida em sua superfície, reavivou-se a discussão sobre a possibilidade de vida em outros sistemas.
Especula-se que as temperaturas na superfície do planeta são semelhantes às da Terra e a pressão atmosférica na sua superfície é estimada como sendo o dobro da pressão na superfície da Terra. A essa pressão, considere que o calor latente de vaporização da água no novo planeta seja 526 cal/g e a água atinja o ponto de ebulição a 120 °C. Calcule a quantidade necessária de calor para transformar 1 kg de água a 25 °C totalmente em vapor naquelas condições, considerando o calor específico da água 1 cal/goC.
22-(MACKENZIE-SP) Para certo procedimento industrial, necessita-se de água a 20 °C, mas só se dispõe de água no estado sólido a 0 °C (gelo) e água fervendo a 100 °C. A relação entre a massa de gelo e a massa de água fervendo que se deve misturar em um recipiente adiabático, para a obtenção do desejado, é
Dados: calor latente de fusão da água = 80 cal/g
calor específico da água líquida = 1 cal/(g°C)
![]()
23-(ITA-SP) Um corpo indeformável em repouso é atingido por um projétil metálico com a velocidade de 300 m/s e a temperatura de 0°C. Sabe-se que, devido ao impacto, 1/3 da energia cinética é absorvida pelo corpo e o restante transforma-se em calor, fundindo parcialmente o projétil. O metal tem ponto de fusão tf = 300°C, calor específico c = 0,02 cal/g°c e calor latente de fusão Lf = 6 cal/g. Considerando 1 cal ¸ 4 J, a fração x da massa total do projétil metálico que se funde é tal que
a) x < 0,25.
b) x = 0,25.
c) 0,25 < x < 0,5.
d) x = 0,5.
e) x > 0,5.
24-(ITA-SP) Um bloco de gelo com 725 g de massa é colocado num calorímetro contendo 2,50 kg de água a uma temperatura de 5,0°C, verificando-se um aumento de 64 g na massa desse bloco, uma vez alcançado o equilíbrio térmico. Considere o calor específico da água (c = 1,0 cal/g°C) o dobro do calor específico do gelo, e o calor latente de fusão do gelo de 80 cal/g. Desconsiderando a capacidade térmica do calorímetro e a troca de calor com o exterior, assinale a temperatura inicial do gelo.
![]()
25-(UFPB) Em um copo há 100g de água (calor específico c=1,0 cal/goC) à temperatura de 30oC. Desejando resfriar a água, coloca-se nesse copo 100g de gelo (calor latente de fusão L=80cal/g) à temperatura de 0oC. Considerando o copo um calorímetro de capacidade térmica desprezível, após o equilíbrio térmico a temperatura será de (em oC):
a) -20
b) -10
c) 0
d) 10
e) 20
26-(UFMA) Certa quantidade de gelo, a temperatura de -7°C foi colocado em um recipiente adiabático, de capacidade térmica desprezível, contendo 500g de água pura a temperatura de 40°C, sob pressao normal. Após algum tempo, a temperatura de equlibrio da mistura estabilizou-se em 30°C. Considerando que cgelo=0,5 cal/g.°C, cágua=1,0cal/g.°C e L=80 cal/g, a massa do gelo em gramas colocada no recipiente foi de, aproximadamente:
![]()
27-(UERJ-RJ) Em casa, é tarefa de a filha encher os recipientes de fazer gelo. Ela pôs 100 g de água, inicialmente a 20 oC, em um dos recipientes e o colocou no freezer, regulado para manter a temperatura em seu interior a −19 0C, sempre que a porta estiver fechada. No entanto, a porta ficou tanto tempo aberta que a temperatura do ar dentro do freezer chegou a − 3 oC.
Sabendo que a pressão atmosférica local é 1 atm, e considerando que o ar no interior do freezer é um gás ideal, determine:
calor específico da água c=4.200J/kg.K — calor latente de solidificação da água=3,3.105Jkg
a) a quantidade de calor que a água do recipiente deve perder para que se converta totalmente em gelo a 0 oC;
b) a pressão no interior do freezer imediatamente após a filha ter fechado a porta.
28-(UNESP-SP) O gálio é um metal cujo ponto de fusão é 30oC à pressão normal; por isso ele pode liquefazer-se inteiramente quando colocado na palma da mão de uma pessoa. Sabe-se que ocalor específico e o calor latente de fusão do gálio são, respectivamente, 410J/kgoC e 80.000Jkg.
a) Qual a quantidade de calor que um fragmento de gálio de massa 25g, inicialmente a 10oC, absorver para fundir-se integralmente quando colocadona palma da mão de uma pessoa?
b) Construa o gráfico t (oC) x Q(J) que representa esse processo supondo que ele comece a 10oC e termine quando o fragmentode gálio se funde integralmente.
29-(UNICAMP-SP) Em um dia quente, um atleta corre dissipando 750 W durante 30 minutos. Suponha que ele só transfira esta energia para o meio externo, através da evaporação do suor, e que todo seu suor seja aproveitado para sua refrigeração.
Adote L = 2 500 J/g para o calor latente de evaporação da água na temperatura ambiente.
a) Qual é a taxa de perda de água no atleta em kg/min?
b) Quantos litros de água ele perde nos 30 min de corrida?
30–(UNIFESP-SP) Em dias muito quentes e secos, como os do último verão europeu, quando as temperaturas atingiram a marca de 40 °C, nosso corpo utiliza-se da transpiração para transferir para o meio ambiente sua energia excedente. Por meio desse mecanismo, a temperatura de nosso corpo é regulada e mantida em torno de 37 °C. No processo de transpiração, a água das gotas de suor sofre uma mudança de fase à temperatura constante, na qual passa lentamente da fase líquida para a gasosa, consumindo energia, que é cedida pelo nosso corpo. Se, nesse processo, uma pessoa perde energia a uma razão de 113 J/s, e se o calor latente de vaporização da água é de 2,26.103 J/g, determine a quantidade de água perdida na transpiração pelo corpo dessa pessoa, em 1 hora.
31-(FGV-SP) Um suco de laranja foi preparado em uma jarra, adicionando-se, a 200mℓ de suco de laranja a 20oC, 50g de gelo fundente. Dados: calor específico da água=1 cal/goC; calor específico do suco de laranja=1 cal/goC; densidade do suco de laranja=1.103g/ℓ; calor latente de fusão do gelo=80cal/g. Estabelecido o equilíbrio térmico, a temperatura do suco gelado era, e, oC, aproximadamente:
a) 0,5
b) 1,2
c) 1,7
d) 2,4
e) 3,3
32-(UFG-GO) Um recipiente de material termicamente isolante contém 300 g de chumbo derretido à sua temperatura de fusão de 327 °C. Quantos gramas de água fervente devem ser despejados sobre o chumbo para que, ao final do processo, toda a água tenha se vaporizado e o metal solidificado se encontre a 100 °C? Suponha que a troca de calor se dê exclusivamente entre a água e o chumbo.
Dados:
calor latente de vaporização da água = 540 cal/g
calor latente de fusão do chumbo = 5,5 cal/g
calor específico do chumbo = 0,03 cal/g °C
![]()
33-(MACKENZIE-SP) No interior de um calorímetro de capacidade térmica desprezível, que contém óleo (c = 0,3 cal/g °C) a 30°C, colocamos uma pedra de gelo (calor latente de fusão = 80 cal/g) de 40 g a 0 °C. A massa de água (calor específico = 1 cal/g °C) a 70 °C que devemos adicionar no calorímetro para restabelecer a temperatura inicial do óleo é de:
a) 80g
b) 90g
c) 100g
d) 110g
e) 150g
34-(ITA-SP) Um vaporizador contínuo possui um bico pelo qual entra água a 20 oC, de tal maneira que o nível de água no vaporizador permanece constante. O vaporizador utiliza 800 W de potência, consumida no aquecimento da água até 100 oC e na sua vaporização a 100 oC. A vazão de água pelo bico é em mililitro por segundo:
Dados: calor específico da água = 1 cal/g °C; calor latente de vaporização da água = 540 cal/g; densidade da água = 1 g/ml; 1 cal = 4,2 J
a) 0,31
b) 0,35
c) 2,4
d) 3,1
e) 3,5
35-(UDESC-SC) O gráfico a seguir representa a variação da temperatura de 200,0 g de água, em função do tempo, ao ser aquecida por uma fonte que libera energia a uma potência constante.
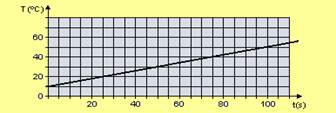
A temperatura da água no instante 135 s e o tempo que essa fonte levaria para derreter a mesma quantidade de gelo a 0°C são respectivamente:
![]()
36-(UNIFESP-SP) 0,50 kg de uma substância a temperatura To = 40°C, na fase líquida, é colocado no interior de um refrigerador, até que a sua temperatura atinja T1 = -10°C. A quantidade de calor transferida em função da temperatura é apresentada no gráfico da figura.
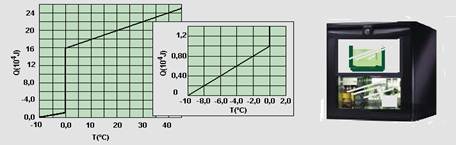
A parte do gráfico correspondente ao intervalo de -10°C a 2,0°C foi ampliada e inserida na figura, à direita do gráfico completo. Calcule:
a) O calor latente específico de solidificação.
b) O calor específico na fase sólida.
37-(UEG-GO) Considere que um bloco de gelo, inicialmente a 0 ºC, seja aquecido a uma taxa constante.
Um tempo t é necessário para transformar o bloco de gelo completamente em vapor d’água a 100 ºC. O que se tem após o tempo t/2?
Considere: calor latente de fusão do gelo = 80 cal/g; calor específico da água = 1 cal/g.°C e calor latente de vaporização da água = 540 cal/g.
a) Água a uma temperatura entre 0 ºC e 100 ºC.
b) Apenas gelo a 0 ºC.
c) Uma mistura de água e vapor a 100 ºC.
d) Uma mistura de gelo e água a 0 ºC.
38-(UNIFESP-SP) Em uma experiência de Termologia, analisou-se a variação da temperatura, medida em graus Celsius, de 100 g de uma substância, em função da quantidade de calor fornecido, medida em calorias. Durante o experimento, observou-se que, em uma determinada etapa do processo, a substância analisada apresentou mudança de fase sólida para líquida. Para visualizar o experimento, os dados obtidos foram apresentados em um gráfico da temperatura da substância como função da quantidade de calor fornecido. Determine: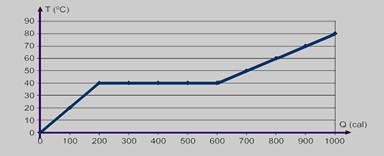
a) O calor específico da substância na fase líquida e seu calor latente específico de fusão.
b) Após a substância atingir a temperatura de 80 ºC, cessou-se o fornecimento de calor e adicionou-se à ela 50 g de gelo a 0 ºC. Supondo que a troca de calor ocorra apenas entre o gelo e a substância, determine a massa de água, fase líquida, em equilíbrio térmico.
Dados:
Calor latente de fusão do gelo: L = 80 cal/g — Calor específico da água: c = 1,0 cal/(g.ºC)
39-(UNICAMP-SP) Em determinados meses do ano observa-se significativo aumento do número de estrelas cadentes em certas regiões do céu, número que chega a ser da ordem de uma centena de estrelas cadentes por hora. Esse fenômeno é chamado de chuva de meteoros ou chuva de estrelas cadentes, e as mais importantes são as chuvas de Perseidas e de Leônidas. Isso ocorre quando a Terra cruza a órbita de algum cometa que deixou uma nuvem de partículas no seu caminho. Na sua maioria, essas partículas são pequenas como grãos de poeira, e, ao penetrarem na atmosfera da Terra, são aquecidas pelo atrito com o ar e produzem os rastros de luz observados.
a) Uma partícula entra na atmosfera terrestre e é completamente freada pela força de atrito com o ar após se deslocar por uma distância de 1 ,5 km . Se sua energia cinética inicial é igual a Ec = 4,5 × 104 J, qual é o módulo da força de atrito média? Despreze o trabalho do peso nesse deslocamento.
b) Considere que uma partícula de massa m = 0,1 g sofre um aumento de temperatura de Dq = 2400 ºC após entrar na atmosfera. Calcule a quantidade de calor necessária para produzir essa elevação de temperatura se o calor específico do material que compõe a partícula é c=0,90J/goC..
40-(PUC-SP) Um cubo de gelo de massa 100 g e temperatura inicial -10 ºC é colocado no interior de um micro-ondas.
Após 5 minutos de funcionamento, restava apenas vapor d’ água. Considerando que toda a energia foi totalmente absorvida pela massa de gelo (desconsidere qualquer tipo de perda) e que o fornecimento de energia foi constante, determine a potência utilizada, em W.
São dados: Pressão local = 1 atm — Calor específico do gelo = 0,5 cal.g.oC-1 — Calor específico da água líquida = 1,0 cal.g.oC-1 — Calor latente de fusão da água = 80 cal. g-1 — Calor de vaporização da água = 540 cal.g-1 — 1 cal = 4,2 J
a) 1.008
b) 896
c) 1.015
d) 903
e) 1.512
41-(PUC-RJ) Uma quantidade de água líquida de massa m = 200 g, a uma temperatura de 30 oC, é colocada em uma calorímetro junto a 150 g de gelo a 0 oC. Após atingir o equilíbrio, dado que o calor específico da água é ca = 1,0 cal/(g . oC) e o calor latente de fusão do gelo é L = 80 cal/g, calcule a temperatura final da mistura gelo + água.
a) 10oC
b) 15 oC
c) 0 oC
d) 30 oC
e) 60 oC
42-(PUC-RJ) Um cubo de gelo dentro de um copo com água resfria o seu conteúdo. Se o cubo tem 10 g e o copo com água tem 200 ml e suas respectivas temperaturas iniciais são 0 oC e 24 oC, quantos cubos de gelo devem ser colocados para baixar a temperatura da água para 20 oC? (Considere que o calor específico da água é ca = 1,0 cal/(g oC), o calor latente de fusão do gelo L = 80 cal/g, e a densidade da água, d = 1 g/ml)
a) 1
b) 2
c) 3
d) 4
e) 5
43-(UNIOESTE-PR) Se misturarmos, num recipiente de capacidade térmica desprezível, 150 g de água a 80ºC com 50 g de gelo a 0ºC, considerando o calor específico da água igual a 1 cal/gºC e o calor de fusão do gelo como 80 cal/g, a temperatura de equilíbrio da mistura será de
![]()
44-(UNICAMP-SP) Na preparação caseira de um chá aconselha-se aquecer a água até um ponto próximo da fervura, retirar o aquecimento e, em seguida, colocar as folhas da planta e tampar o recipiente. As folhas devem ficar em processo de infusão por alguns minutos. Caso o fogo seja mantido por mais tempo que o necessário, a água entrará em ebulição. Considere que a potência fornecida pelo fogão à água é igual a 300 W, e que o calor latente de vaporização da água vale 2,25 x 103 J/g. Mantendo-se o fogo com a água em ebulição e o recipiente aberto, qual é a massa de água que irá evaporar após 10 minutos?
a) 18 g.
b) 54 g.
c) 80 g.
d) 133 g.
45-(UECE-CE) Considerando que os calores específico e latente de vaporização da água são respectivamente c = 4.190 J/kg.K e L = 2.256 kJ/kg, a energia mínima necessária para vaporizar 0,5 kg de água que se encontra a 30ºC, em kJ, é aproximadamente:
![]()
46–(UFAC-AC) Em geral, a temperatura do ser humano é constante e igual a 37°C. A hipotermia é caracterizada pela redução da temperatura padrão de nosso corpo. A Medicina faz o uso controlado da hipotermia, em determinadas cirurgias cerebrais e
cardíacas. Esse procedimento diminui o consumo de oxigênio do cérebro e do coração, bem como reduz a chance de danos ocasionados pela falta de circulação do sangue. Suponha que um paciente, de massa 60 kg, seja submetido a uma cirurgia de coração. A temperatura inicial de seu corpo é 37°C e pretende-se diminuí-la para 30°C. Considere o calor específico do corpo humano igual a 1,0 cal/g.°C e o calor latente de fusão do gelo igual a 80 cal/g. A massa mínima de gelo necessária para diminuir a temperatura do paciente até 30°C é:
![]()
47-(ENEM-MEC)

Em nosso cotidiano, utilizamos as palavras “calor” e “temperatura” de forma diferente de como elas são usadas no meio científico. Na linguagem corrente, calor é identificado como “algo quente” e temperatura mede a “quantidade de calor de um corpo”. Esses significados, no entanto, não conseguem explicar diversas situações que podem ser verificadas na prática.
Do ponto de vista científico, que situação prática mostra a limitação dos conceitos corriqueiros de calor e temperatura?
a) A temperatura da água pode ficar constante durante o tempo em que estiver fervendo.
b) Uma mãe coloca a mão na água da banheira do bebê para verificar a temperatura da água.
c) A chama de um fogão pode ser usada para aumentar a temperatura da água em uma panela.
d) A água quente que está em uma caneca é passada para outra caneca a fim de diminuir sua temperatura.
e) Um forno pode fornecer calor para uma vasilha de água que está em seu interior com menor temperatura do que a dele.
48-(UNICAMP-SP)

Na preparação caseira de um chá aconselha-se aquecer a água até um ponto próximo da fervura, retirar o aquecimento e, em seguida, colocar as folhas da planta e tampar o recipiente. As folhas devem ficar em processo de infusão por alguns minutos.
Caso o fogo seja mantido por mais tempo que o necessário, a água entrará em ebulição. Considere que a potência fornecida pelo fogão à água é igual a 300 W, e que o calor latente de vaporização da água vale 2,25.103 J/g. Mantendo-se o fogo com a água em ebulição e o recipiente aberto, qual é a massa de água que irá evaporar após 10 minutos?
a) 18 g.
b) 54 g.
c) 80 g.
d) 133 g.
49-(UEPG-PR)

No que se refere à mudança de estado da matéria, assinale o que for correto.
01) A quantidade de calor por grama necessária para que ocorra a mudança de estado é denominada de calor latente. Essa propriedade pode ser utilizada para diferenciar os materiais, adequando-os a seus diferentes usos.
02) A temperatura de mudança de estado é influenciada pela pressão a que a substância está submetida.
04) Tanto a vaporização como a condensação são processos que ocorrem por meio de troca de energia entre a substância e o meio no qual ela se encontra.
08) A evaporação ocorre a qualquer temperatura, mas a velocidade de evaporação do líquido aumenta com a elevação da temperatura.
50-(IFSP-SP)

Um estudante de física, ao nível do mar, possui um aquecedor de imersão de 420 W de potência e o coloca dentro de uma panela contendo 2 litros de água a 20°C. Supondo que 80% da energia dissipada seja absorvida pela água, o intervalo de tempo necessário para que 20% dessa água seja vaporizada será aproximadamente de
Dados:
calor específico da água: 1,0 cal/g°C
Calor Latente de vaporização da água: 540 cal/g
Densidade absoluta da água: 1,0 kg/L
1 cal = 4,2 J
a) 1 h e 13 minutos.
b) 1 h e 18 minutos.
c) 1 h e 25 minutos.
d) 1 h e 30 minutos.
e) 2 h e 10 minutos.
51-(FUVEST-SP)

Um forno solar simples foi construído com uma caixa de isopor, forrada internamente com papel alumínio e fechada com uma tampa de vidro de 40 cm x 50 cm. Dentro desse forno, foi colocada uma pequena panela contendo 1 xícara de arroz e 300 mL de água à temperatura ambiente de 25°C.

Suponha que os raios solares incidam perpendicularmente à tampa de vidro e que toda a energia incidente na tampa do forno a atravesse e seja absorvida pela água. Para essas condições, calcule:
a) A potência solar total P absorvida pela água.
b) A energia E necessária para aquecer o conteúdo da panela até 100°C.
c) O tempo total T necessário para aquecer o conteúdo da panela até 100°C e evaporar 1/3 da água nessa temperatura (cozer o arroz).

52-(PUC-RJ)

Um copo com 300 ml de água é colocado ao sol. Após algumas horas, verifica-se que a temperatura

da água subiu de 10 °C para 40 °C. Considerando-se que a água não evapora, calcule em calorias a quantidade de calor absorvida pela água.
Dados: dágua=1g/cm3 e c=1cal/goC
(A) 1,5.105
(B) 2,0.105
(C) 3,0.103
(D) 9,0.103
(E) 1,2.102
53-(UFMG-MG)

01- Um copo com 200 g de água está inicialmente a 25oC. Carolina coloca 50 g de gelo, a 0oC, nesse copo.

Após algum tempo, todo o gelo derrete e toda água no copo está à mesma temperatura.
01. Considerando o sistema água e gelo isolado, calcule a temperatura no instante em que esse sistema chega ao equilíbrio térmico.
02- Assinalando com um X a quadrícula apropriada, responda:
Considerando-se, agora, o sistema isolado como água, gelo e copo, o valor obtido para a temperatura do sistema será menor, igual ou maior ao valor obtido no item 1, desta questão?
![]()
Justifique sua resposta.
54-(MACKENZIE-SP)

Um estudante, no laboratório de Física de sua escola, forneceu calor a um corpo de massa 50 g, utilizando uma fonte térmica de potência
constante. Com as medidas obtidas, construiu o gráfico ao lado, que representa a quantidade de calor ∆Q recebida pelo corpo em função de sua temperatura t.
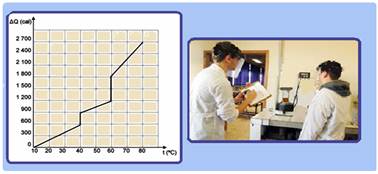
Analisando o gráfico, pode-se afirmar que o calor específico, no estado sólido e o calor latente de vaporização da substância que constitui o corpo, valem, respectivamente,
a) 0,6 cal/(g.ºC) e 12 cal/g
b) 0,4 cal/(g.ºC) e 12 cal/g
c) 0,4 cal/(g.ºC) e 6 cal/g
d) 0,3 cal/(g.ºC) e 12 cal/g
e) 0,3 cal/(g.ºC) e 6 cal/g
55-COLÉGIO NAVAL-011-012)

Durante uma expedição ao Polo Sul, um pesquisador precisou usar água líquida

na temperatura de 50°C para fazer um determinado experimento.
Para isso pegou 2kg de gelo que se encontravam à temperatura de -20oC e colocou uma fonte térmica fornecia 20 kcal/min.
Qual foi o tempo, em unidades do Sistema Internacional, que o pesquisador esperou para continuar o seu experimento?
Dados: calor específico do gelo = 0,5 cal/g°C; calor específico da água = 1 cal/g°C e calor latente de fusão do gelo = 80 cal/g
(A) 500
(B) 640
(C) 720
(D) 840
(E) 900
